维通达深耕于肝病研究领域二十余年,建立了在自主研发的可诱导肝损伤的免疫缺陷小鼠URG和NPG-Fah小鼠上移植原代人肝细胞(PHH)、培养扩增的人肝细胞以及诱导分化来的类肝细胞的技术,以手术方式结合一整套肝损伤诱导方案、围术期监护、检测分析手段等,获得人肝细胞替换率高达90%以上的人源化嵌合肝脏小鼠,可提供此类技术服务。除此之外,维通达建立了在自主研发的B6-Fah小鼠上移植同背景原代小鼠肝细胞或类肝细胞移植技术,可提供此类技术服务。维通达可提供的服务包括:
1. 原代或培养扩增的人肝细胞以及诱导分化来的类肝细胞移植
2. 鼠肝细胞移植
案例一:URG®小鼠用于验证功能性肝细胞(EPS-Heps)在体内的再生能力[1]
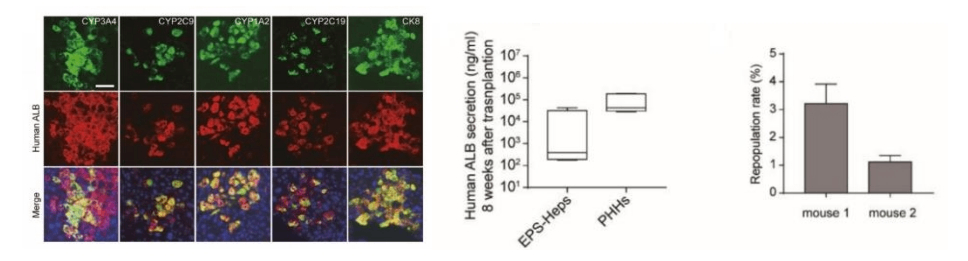
图1. URG®小鼠移植EPS-Heps与PHHs 8周后人肝细胞重建情况
URG®小鼠移植EPS-Heps 8周后,检测到人CYP3A4、CYP2C9、CYP1A2和CYP2C19与人ALB 共表达,同时血清中检测到人ALB的分泌。这些数据表明,EPS-Heps是具有功能成熟特征的类肝细胞,可以重建受损小鼠肝脏。
案例二:URG®小鼠用于肝样细胞(HLC)移植治疗肝功能衰竭[2]
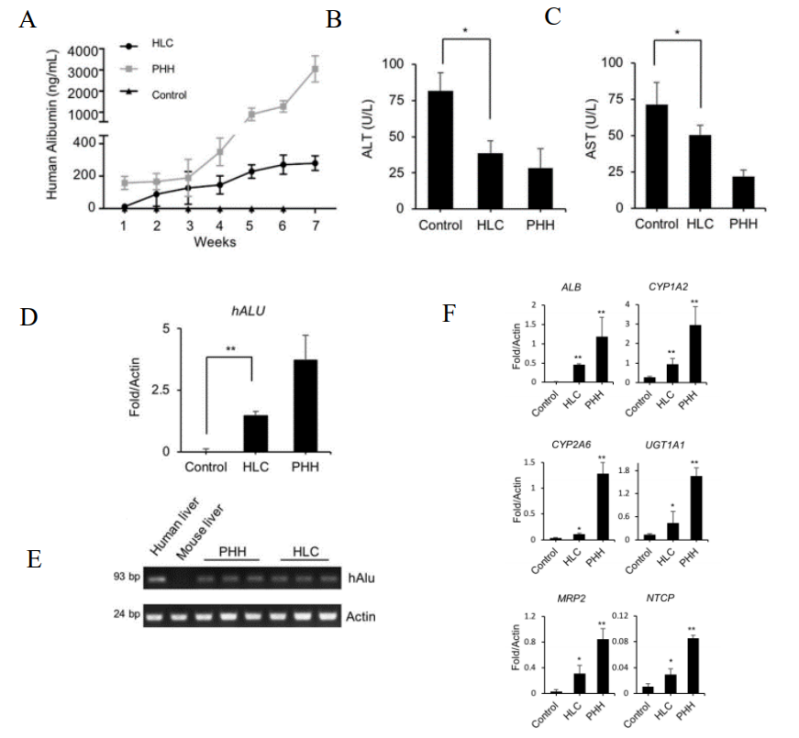
图2. URG®小鼠移植HLC后肝细胞再生
8 周龄雄性小鼠(n=5/group)在细胞移植前12小时通过腹腔注射15 mg/kg体重的强力霉素(Dox),以PBS作为对照,把HLC、PHHs,经脾内移植到小鼠体内。细胞移植后URG®小鼠持续饲喂含Dox饮用水6周。每周尾静脉取血,用ELISA法定量测定人ALB水平,第7周处死。结果表明:URG®小鼠移植HLC后小鼠血清中人ALB分泌量逐渐增加,7周后血清ALT和AST浓度显著降低,人特异性ALU序列的实时PCR进一步证实了HLC在小鼠肝脏中的定植。同时检测到嵌合肝组织人类特异性基因ALB、人类肝细胞特异性代谢基因I期酶CYP1A2和CYP2A6等的表达。这些数据表明HLC可以整合到URG®小鼠肝脏中,改善肝功能障碍。
案例三:URG®小鼠用于体外转分化肝脏细胞功能的体内验证试验[3]
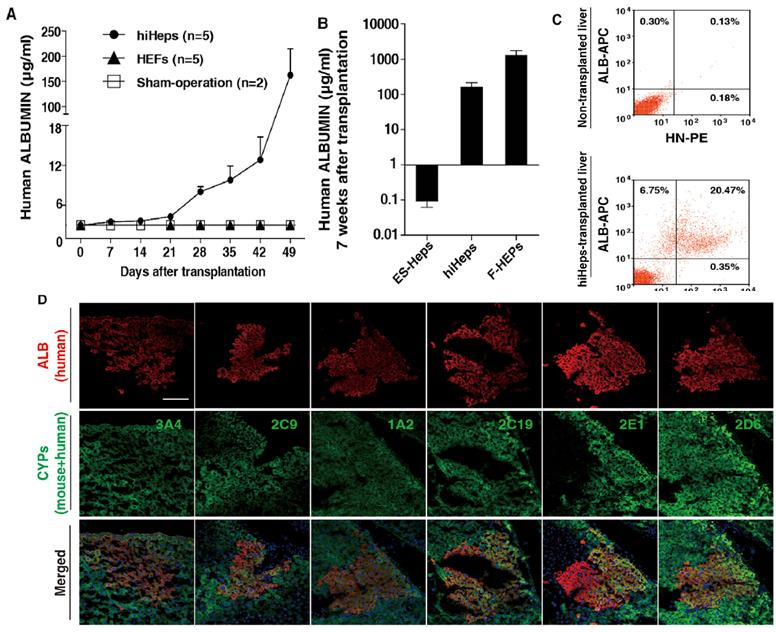
图3. URG®小鼠移植人诱导肝细胞(hiHeps)后肝细胞再生
URG®小鼠脾内注射ES-Heps (n=16)、hiHeps (n=5)和 F-HEPs (n=6)。采集血样,ELISA法对人ALB进行定量,对肝脏切片染色及流式分析等操作。结果表明:URG®小鼠移植hiHeps后小鼠血清中人白蛋白分泌量逐渐增加,移植6周后移植小鼠肝脏中观察到表达人ALB细胞簇。同时证实 hiHeps在体内的代谢功能,分析了CYP3A4、CYP2C9等表达。表明hiHeps在体内可稳定生长并具有功能。本研究说明URG®小鼠可用于验证hiHeps作为肝细胞移植的潜在细胞来源。
维通达优势:
(1)URG®小鼠的优点是,不诱导时uPA并不表达,小鼠健康生长;当用Dox诱导时,Tet-On系统驱动的uPA即在肝内表达,小鼠出现肝损伤,此时可接受外源肝细胞的植入。人源肝细胞移植可以在URG®小鼠实现高达90%的整肝重建,且移植窗口期不受限制。
(2)相较于Fah敲除鼠,用URG®鼠移植肝细胞,肝重建周期短(URG需6~9周,Fah KO鼠需3~6个月),节约实验时间。相较于恒定表达uPA的小鼠,URG®小鼠体重更大,成体雄鼠31±3 g,肝细胞移植手术后体重维持在25±3 g。因而肝重建成功的Hu-URG®小鼠健康状态好,对实验操作的耐受力更好。
参考文献:
1. Wang Q, Sun D, Liang Z, et al. Generation of human hepatocytes from extended pluripotent stem cells. Cell Res. 2020, 30:810-813.
2. Li Z, Wu J, Wang L, et al. Generation of qualified clinical-grade functional hepatocytes from human embryonic stem cells in chemically defined conditions. Cell Death Dis. 2019, 10:763.
3. Du Y, Wang J, Jia J, et al. Human hepatocytes with drug metabolic function induced from fibroblasts by lineage reprogramming. Cell Stem Cell. 2014, 14:394-403.