基本信息
品系名称 | NOD.Cg-Tg(tetO-Alb-uPA)1Deng Rag2tm1Il2rgtm1/Vst |
常用名 | URG®小鼠;Tet-uPATgRag2null Il2rgnull小鼠 |
来源 | 北京维通达生物技术有限公司 |
背景 | NOD |
毛色 | 白色 |
品系建立
URG小鼠由4种基因修饰动物模型交配获得,包含2个转基因和2个基因敲除。构建方式如下:
首先,TRE-uPA转基因小鼠与Alb-rtTA转基因小鼠交配获得Alb-rtTA/TRE-uPA双阳性小鼠,通过Dox诱导,在该小鼠肝脏中检测到uPA表达和肝损伤[1];其次,Alb-rtTA/TRE-uPA双阳性小鼠连续8代回交到NRG(NOD背景的Rag2nullIl2rgnull小鼠) 背景,获得Alb-rtTA/TRE-uPA/Rag2null/Il2rgnull小鼠(URG)。URG不诱导时uPA并不表达,小鼠健康生长;当用doxycycline (Dox)诱导时,Tet-On系统驱动的uPA即在肝内表达,小鼠出现肝损伤。
表型信息
1. 肝损时间可调控
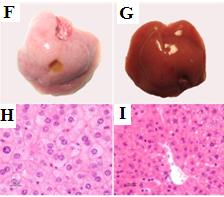
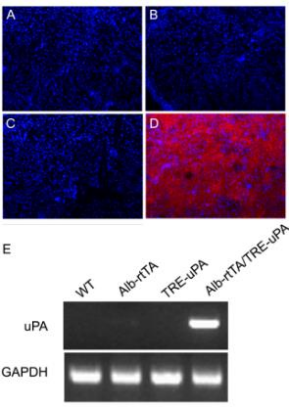
图1. URG®小鼠肝损伤分析
URG®同NPG小鼠一样常规扩繁,可以在任何时间用Dox诱导肝损伤。在不诱导时,检测不到表达uPA表达(C);在Dox诱导后,免疫组化可检测到uPA表达(D);uPA表达的肝脏呈苍白色(F);野生型小鼠的肝脏是暗红色(G);HE染色可见URG®小鼠肝细胞肿胀和空泡化(H);对照小鼠肝细胞形态正常(I)。
2. URG®肝损伤后血清学指标[2]
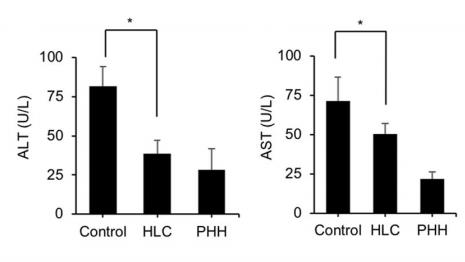
图2. URG®小鼠在Dox饮水诱导下ALT和AST的血清水平(n=5/group)
注:将肝样细胞(HLC)、原代人肝细胞(PHHs)、PBS作为对照,分别经脾内移植到小鼠体内。移植7周后血清ALT和AST水平测定
URG®小鼠研究实例
1. 验证功能性肝细胞(EPS-Heps)在体内的再生能力[3]
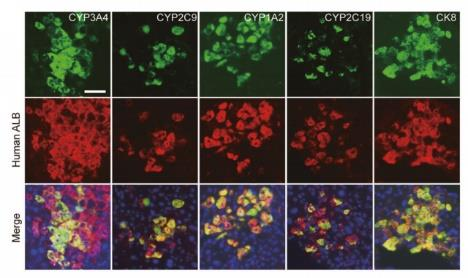
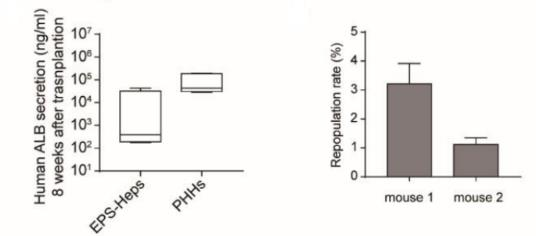
图3. URG®小鼠移植EPS-Heps与PHHs 8周后人肝细胞重建情况
URG®小鼠移植EPS-Heps 8周后,检测到人CYP3A4、CYP2C9、CYP1A2和CYP2C19与人Alb 共表达,同时血清中检测到人Alb的分泌。这些数据表明,EPS-Heps可以重建具有功能成熟特征的受损小鼠肝脏。
2. 用于肝细胞样细胞(HLC)移植治疗肝功能衰竭[2]
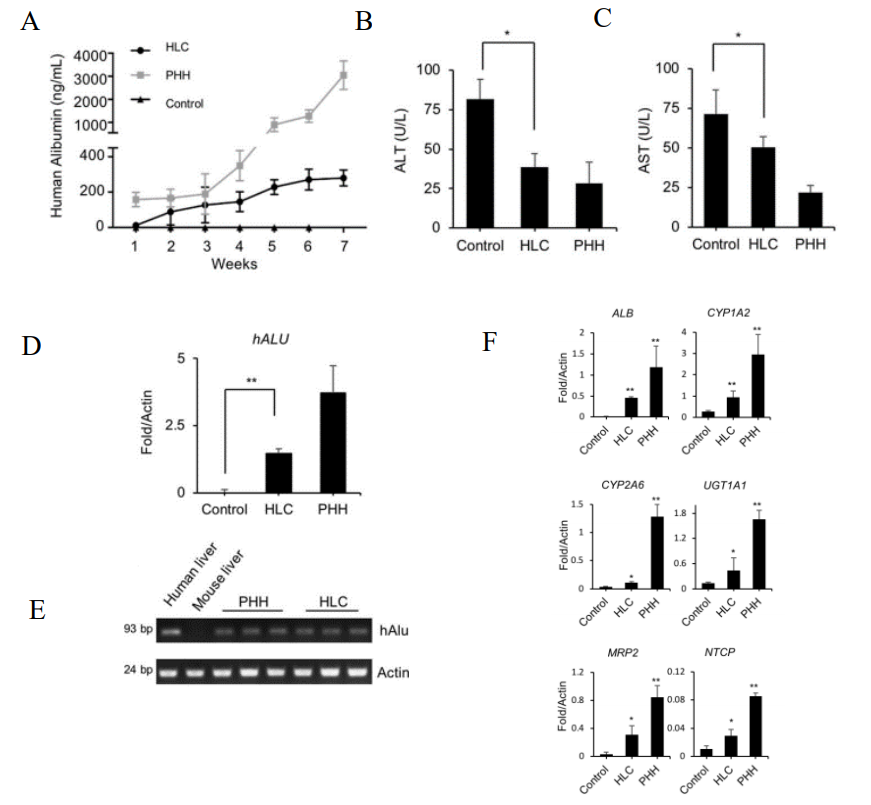
图4. URG®小鼠移植HLC后肝细胞再生
8 周龄雄性小鼠(n=5/group)在细胞移植前12小时通过腹腔注射15 mg/kg体重的Dox,以PBS作为对照,把HLC、PHHs,经脾内移植到小鼠体内。细胞移植后URG®小鼠持续饲喂含Dox饮用水6周。每周尾静脉取血,用ELISA法定量测定人ALB含量,第7周处死。结果表明:URG®
小鼠移植HLC后,血清中人ALB分泌量逐渐增加,7周后血清ALT和AST浓度显著降低,人特异性ALU序列的实时PCR进一步证实了HLC在小鼠肝脏中的定植。同时检测到人类特异性基因ALB、人类肝细胞特异性代谢基因I期酶CYP1A2和CYP2A6等。这些数据表明HLC可以整合到URG®小鼠肝脏中,改善肝功能障碍。
3. 体外转分化肝脏细胞功能的体内验证试验[4]
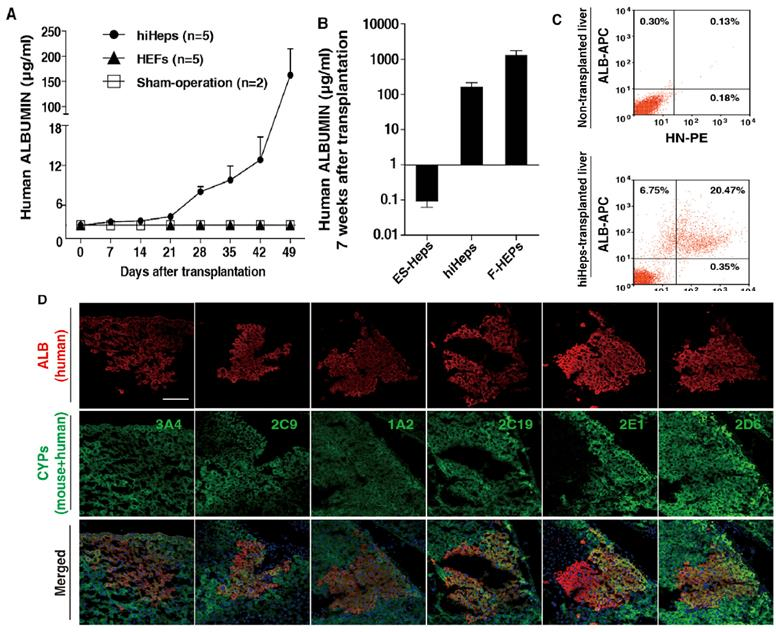
图5. URG®小鼠移植人诱导肝细胞(hiHeps)后肝细胞再生
URG®小鼠脾内注射ES-Heps (n=16)、hiHeps (n=5)和 F-HEPs (n=6)。采集血样,ELISA 法对人Alb进行定量,对肝脏切片染色及流式分析等操作。结果表明:URG®小鼠移植hiHeps后小鼠血清中人Alb分泌量逐渐增加,移植6周后,观察到小鼠表达人Alb细胞簇。同时证实 hiHeps在体内的代谢功能,分析了CYP3A4、CYP2C9等表达。表明 hiHeps 在体内可稳定生长并具有功能。本研究说明URG®小鼠可用于验证hiHeps作为肝细胞移植的潜在细胞来源。
URG®小鼠应用领域
1. 可构建调控肝损伤和人源化肝脏损伤模型,用于人特异的肝病、药物安全性评估和人特异的肝脏代谢酶相关的研究
2. HBV,HCV感染及抗病毒活性信号通路研究
3. 药物代谢与药代动力学、药效研究
4. 干细胞研究
5. 基因治疗
参考文献
1. Song X J, et al. A Mouse Model of Inducible Liver Injury Caused by Tet-On Regulated Urokinase for Studies of Hepatocyte Transplantation. Am J Pathol. 2009, 175(5):1975-1983.
2. Li Z, et al. Generation of qualified clinical-grade functional hepatocytes from human embryonic stem cells in chemically defined conditions. Cell Death Dis. 2019, 10:763.
3. Wang Q, et al. Generation of human hepatocytes from extended pluripotent stem cells. Cell Res. 2020, 30:810-813.
4. Du Y, et al. Human hepatocytes with drug metabolic function induced from fibroblasts by lineage reprogramming. Cell Stem Cell. 2014, 14(3):394-403.