基本信息
品系名称 | HBV-Hu-URG |
来源 | 北京维通达生物技术有限公司 |
背景 | URG |
毛色 | 白色 |
品系建立
HBV-HuURG即感染HBV的人源化肝脏小鼠的模型。
人原代肝细胞移植的URG小鼠产生的人鼠嵌合肝脏小鼠(人源化肝脏小鼠),可以被来自乙肝病人或体外制备的HBV病毒感染。由于在小鼠肝脏中有人类肝脏细胞的存在,因而可以复现HBV自然感染和复制过程,肝细胞中有cccDNA存在。相较HBV-Tg小鼠或AAV-HBV小鼠,HBV-HuURG小鼠是真正的HBV感染模型,在HBV感染机理研究、抗HBV药物研发领域具有更大应用价值。
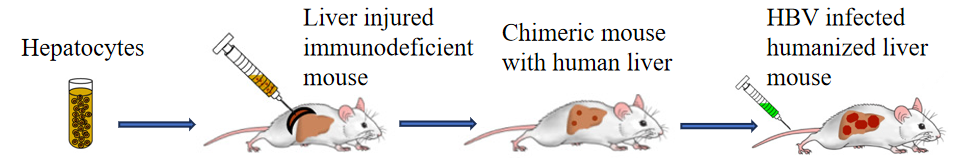
图1. HBV感染Hu-URG小鼠示意图
表型信息
1. 感染A型HBV病毒不同时间各HBV指标
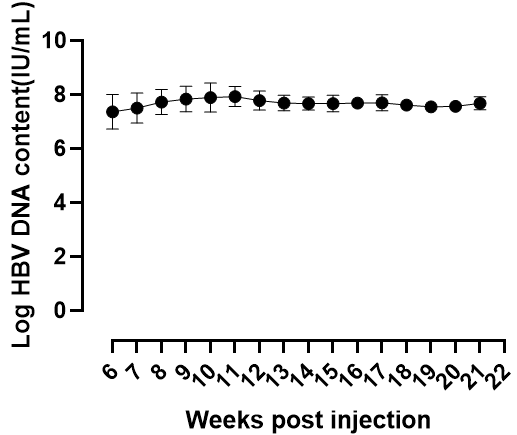
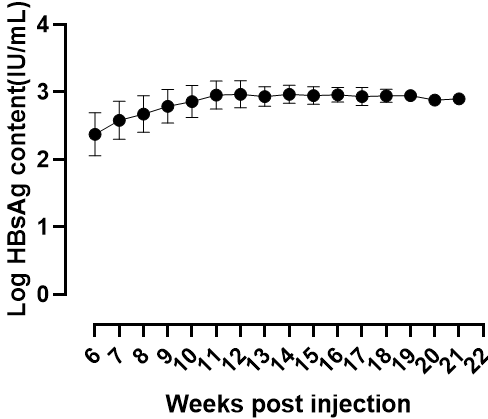
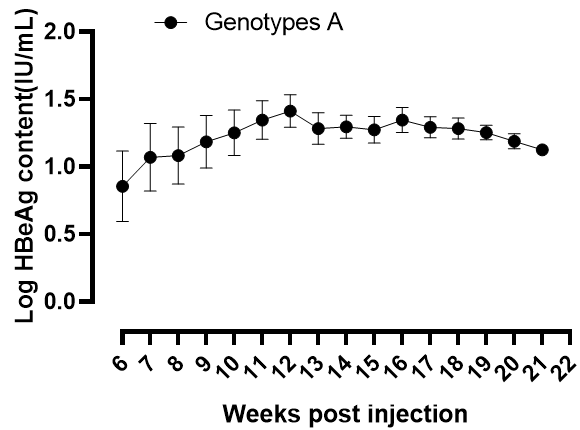
图2. HBV-Hu-URG小鼠外周血HBV各指标检测
2. 人肝细胞重建水平
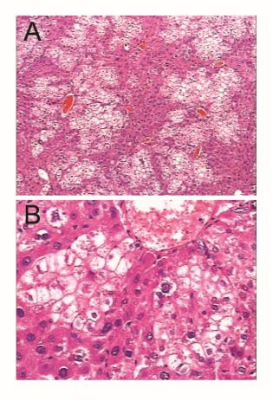
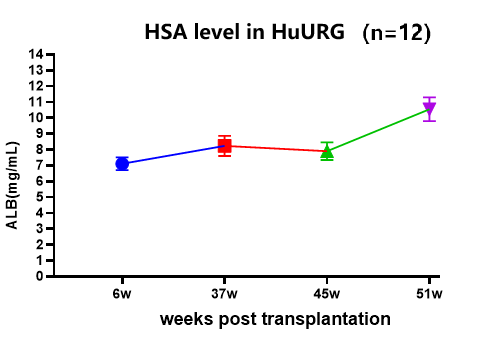
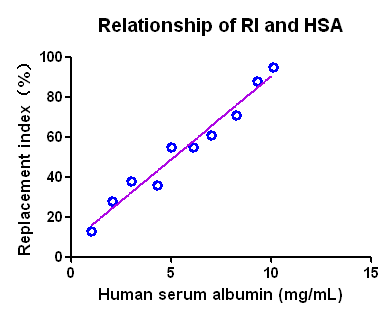
图3. Hu-URG小鼠人肝细胞重建
注:(A,B) HE 染色证明人肝细胞在 Hu-URG小鼠肝脏中重建成功,染色浅的部分为人肝脏细胞;(C) Hu-URG的外周血人Alb 水平;(D) Hu-URG外周血Alb水平与人肝细胞嵌合程度相关性分析
结果表明:Hu-URG小鼠在感染HBV后25周内的人白蛋白水平高于1 mg/mL,在这一周期内任何时间均可感染HBV病毒,实验窗口期可达25周。
3. 不同基因型HBV感染HuURG小鼠血清HBV DNA拷贝数与肝组织指标
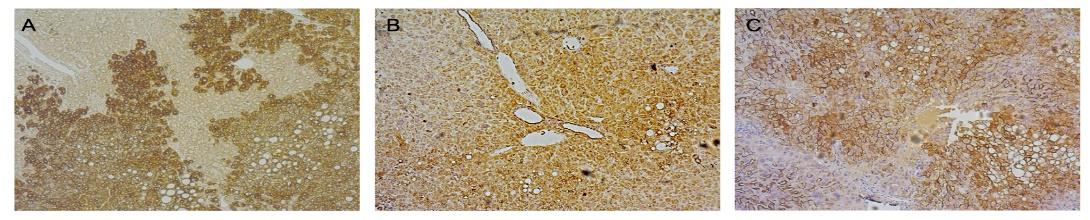
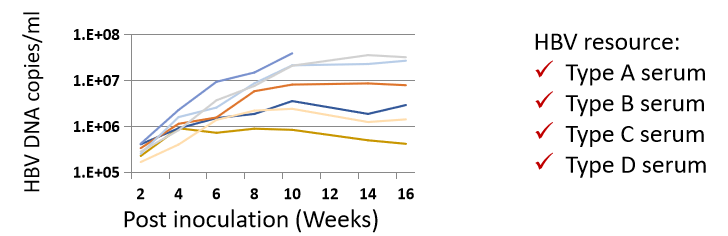
图4. 不同基因型HBV感染HuURG小鼠血清与肝组织指标检测
注:A为Human CK18,B为HBcAg,C为HBsAg
Hu-URG小鼠感染HBV及药效研究实例
1. Hu-URG用于研究HBV患者血清感染后小分子化合物抗病毒活性及其对cccDNA转录的潜在影响机制[1]
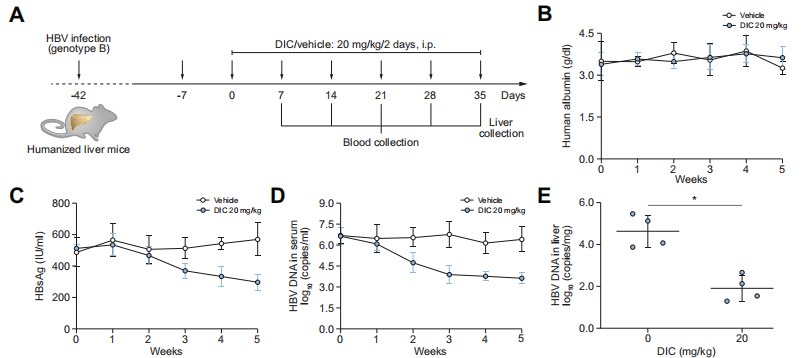
图7. Dicoumarol 对 HBV 感染 Hu-URG 小鼠的抗病毒活性
Hu-URG小鼠(n=4/group)静脉注射50 μL HBV患者血清(基因型B, 5.12×106 copies/mL)。6周后,每隔一天腹腔注射20 mg/kg Dicoumarol, 同时设置对照组。每周眼眶静脉窦取血。给药35 d后处死小鼠,收集肝脏组织进行分析。结果表明:Hu-URG小鼠血清中Alb一直处于较高水平。在给药Dicoumarol治疗的5周内高于3 mg/mL,与对照组无显著差异。Dicoumarol处理可有效降低血清HBsAg和HBV DNA水平,并降低肝内HBV DNA和HBV RNAs水平。
2. Hu-URG小鼠用于研究培养的HBV病毒颗粒感染后化合物抗病毒活性及其对cccDNA转录影响[2]
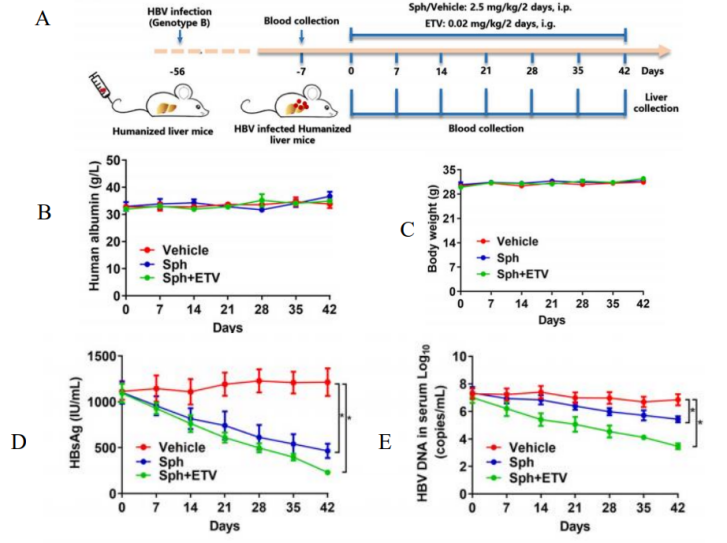
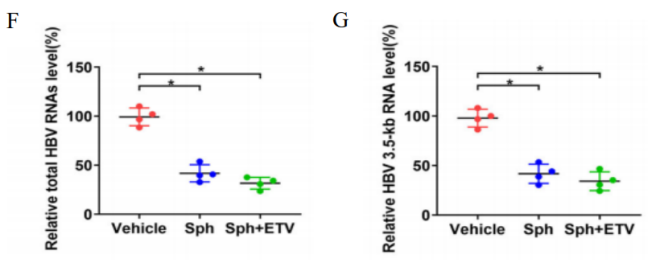
图8. Sphondin对HBV感染Hu-URG小鼠的抗病毒活性
Hu-URG小鼠(n=4/group)静脉注射患者血清(基因型B)。8周后,将小鼠随机分为对照组、sphondin单药治疗组和ETV+sphondin 联合组,按照如图设计给药取材。结果表明:Hu-URG小鼠血清中人Alb一直处于较高水平。在单独或联合给药治疗的6周内高于3 mg/mL,与对照组无显著差异。给药处理对体重也无显著影响。sphondin治疗可使血清 HBsAg和HBV DNA显著降低。同样也能显著降低肝内总HBV RNA、3.5 kb RNA、HBsAg和HBx蛋白水平。
3. Hu-URG用于研究HBx通过DDB1介导的WDR77在肝脏中的降解增强HBV复制[3]
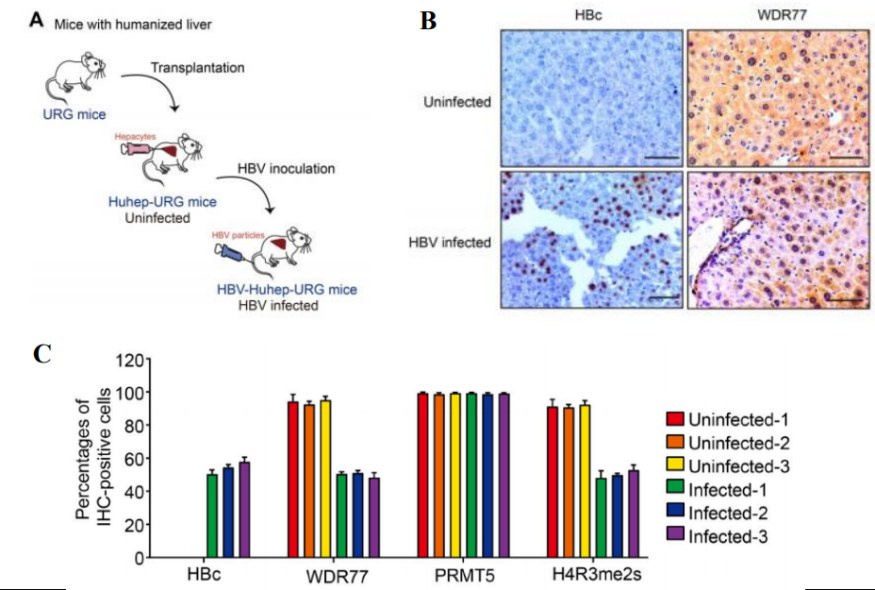

图9. HBV感染导致WDR77水平下降
PHHs通过脾内注射至3周龄URG小鼠中(n=3/group),ELISA法测定血清人Alb,评估PHHs的植入和活力。然后用2.5×108 IU/mL (0.2 mL/只)HBV颗粒感染小鼠,8周后处死小鼠。结果表明:Hu-URG小鼠血清中Alb处于较高水平且可正常感染HBV,HBV感染和 HBx表达显著降低了Hu-URG 的WDR77的蛋白水平,进而限制cccDNA转录和HBV复制。
4. Hu-URG用于研究药物治疗慢性乙肝的潜在靶点[4]
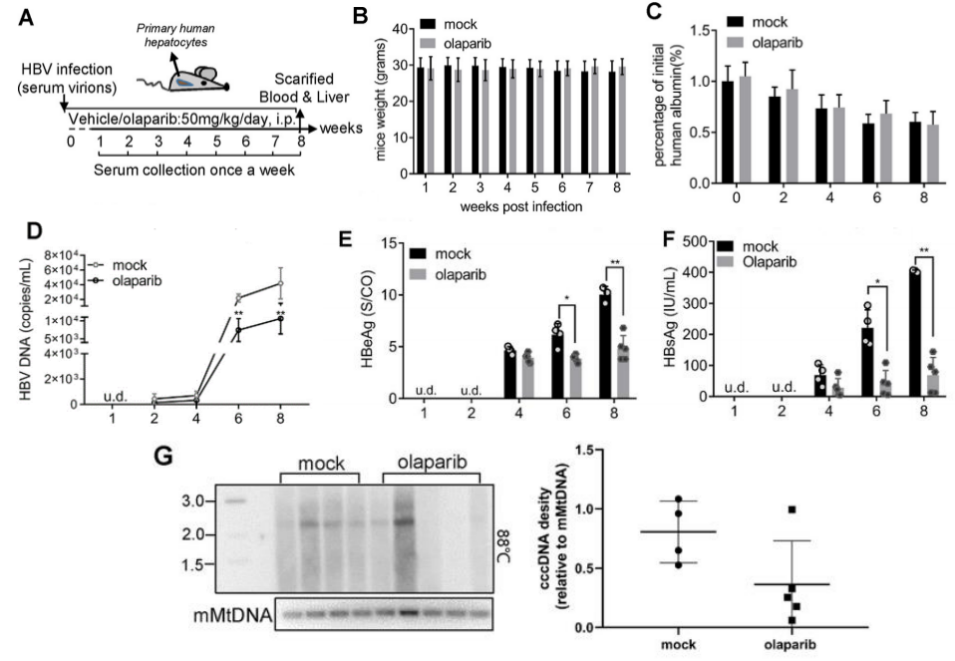
图10. PARP1 抑制剂(olaparib)处理的 Hu-URG 小鼠 HBV cccDNA 减少
9只雄性小鼠(n=4 male mice in mock group, n=5 male mice in olaparib group)静脉注射 HBV患者血清50 μL (5×108 copies/mL)。在HBV感染12小时后以每天50 mg/kg的剂量腹腔给药稀释的PARP1抑制剂olaparib。结果表明:Hu-URG在DMSO组和olaparib组的体重和血清人Alb水平无显著差异。给药后血清HBV DNA、HBsAg和HBeAg水平显著降低。肝内 HBV cccDNA水平降低一半。这些数据表明olaparib可减少体内HBV复制和cccDNA的形成。
5. Hu-URG用于研究IFN-α介导HDAC3抑制HBV转录和复制的通路研究[5]
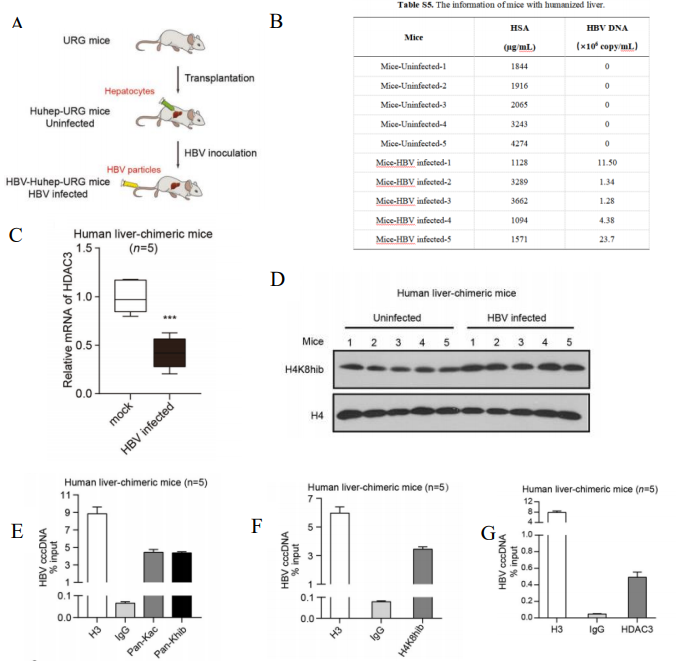
图11. HDAC3 介导抑制 HBV 转录和复制
原代人肝细胞(PHH)移植到3周龄(n=5 each group, male and female)经Dox诱导的肝损伤的URG小鼠,构建产生Hu-URG小鼠。酶联免疫吸附测定法测定血清人Alb白蛋白,以评估 PHH 的植入和活力。然后用来自HepAD38细胞上清液5.0×108 IU/mL (0.2mL/小鼠)HBV 颗粒感染Hu-URG小鼠。结果表明:人肝嵌合小鼠血清中Alb处于较高水平且可正常感染 HBV,感染HBV的Hu-URG小鼠中的HDAC3 mRNA水平较对照组显著降低,Western blot分析证实组蛋白H4K8 2-羟基异丁酰化水平明显增强。ChIP 分析显示,HDAC3与HBV 感染的 Hu-URG小鼠肝脏中的HBV cccDNA结合,这表明 HDAC3锚定在 HBV cccDNA 染色体上。本研究发现IFN-α 通过促进HDAC3介导的肝脏HBV cccDNA染色体上组蛋白H4K8的去2-羟基异丁酰化来抑制HBV转录和复制。
HBV-Hu-URG小鼠应用领域
1. HBV-Hu-URG小鼠可用于研究HBV药物安全性评估和人特异的肝脏代谢酶相关的研究
2. HBV,HCV感染及抗病毒活性信号通路研究
3. 药物代谢与药代动力学、药效研究
4. 干细胞研究
5. 基因治疗
参考文献
1. Cheng ST, et al. Dicoumarol, an NQO1 inhibitor, blocks cccDNA transcription by promoting degradation of HBx. J Hepatol. 2021, 74:522-534.
2. Ren F, et al. Sphondin efficiently blocks HBsAg production and cccDNA transcription through promoting HBx degradation. J Med Virol. 2023, 95:e28578.
3. Yuan H, et al. HBx represses WDR77 to enhance HBV replication by DDB1-mediated WDR77 degradation in the liver. Theranostics. 2021, 11(17):8362-8378.
4. Chen Y, et al. DNA Repair Factor Poly (ADP-Ribose) Polymerase 1 Is a Proviral Factor in Hepatitis B Virus Covalently Closed Circular DNA Formation. J Virol. 2022, 96(13):e0058522.
5. Zhao LN, et al. IFN-α inhibits HBV transcription and replication by promoting HDAC3-mediated de-2-hydroxyisobutyrylation of histone H4K8 on HBV cccDNA minichromosome in liver. Acta Pharmacol Sin. 2022, 43(6):1484-1494.