肿瘤免疫双人源化:肿瘤免疫双人源化(dual humanized)小鼠模型通常是指在免疫缺陷小鼠中同时植入人类肿瘤细胞和人类免疫系统,创建一个同时包含人类免疫系统和肿瘤的研究平台。该模型具有更高的临床相关性、多样性和灵活性。
更好的临床相关性体现为相比于传统的肿瘤异种移植模型,双人源化模型包含了人类免疫系统,使得研究结果更具临床相关性。其次是能够研究更复杂的肿瘤-免疫相互作用,提供对肿瘤生物学和免疫机制的更全面理解;多样性和灵活性体现为适用于多种肿瘤类型和免疫治疗的研究,提供了一个灵活的研究平台。同时可以根据研究需要选择不同的肿瘤和免疫细胞类型,定制化研究模型。
我们维通达自主研发的肿瘤免疫双人源化小鼠模型为癌症研究提供了一个强大的工具,能够更准确地模拟人类肿瘤和免疫系统的相互作用,为免疫疗法的开发、药物筛选和个性化医学研究提供了重要的平台。
(1)肿瘤免疫双人源化经验丰富
1. 构建人胃癌模型及胃癌间充质干细胞联合PD-1抗体药体内药效[1]
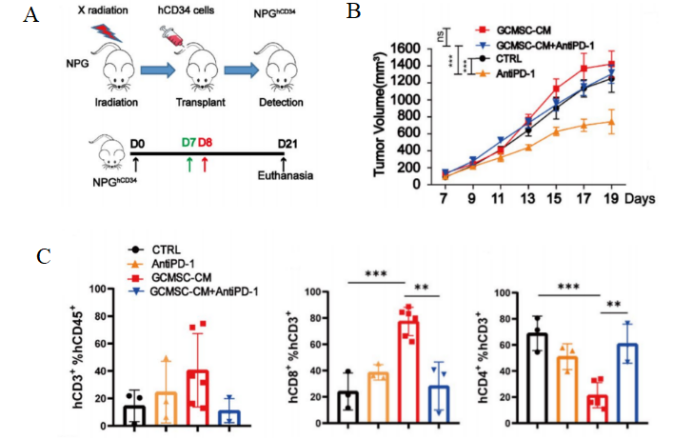
图1. Hu-HSC-NPG接种胃癌肿瘤后肿瘤及肿瘤组织免疫细胞水平
4-8周龄NPG小鼠经X射线(1.2 Gy)照射后24 h内静脉注射5×104人脐带血CD34+细胞。重建12周之后接种患者胃癌肿瘤细胞系,并分别或联合使用GCMSC-CM和PD-1抗体治疗并观测肿瘤变化,并检测不同处理组肿瘤组织中CD45+CD3+, CD3+CD8+, CD3+CD4+含量。结果表明:在治疗后21天,PD-1抗体治疗显著抑制胃肿瘤生长,而GCMSC-CM联合PD-1抗体比单独使用PD-1抗体治疗显著增加肿瘤体积,说明GCMSC-CM消除了PD-1抗体对胃肿瘤生长的抑制作用。
2. 构建人淋巴瘤模型及小分子抑制剂药效[2]
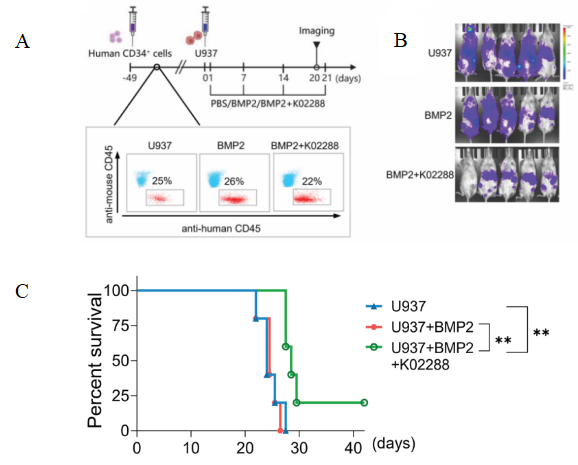
图2. Hu-HSC-NPG接种U937细胞系构建示意图及抗肿瘤效果
5-6周龄雌性NPG小鼠(n=5 per group)辐照(1 Gy)清髓之后尾静脉注射5×105人CD34+细胞,6-7周后外周血检测anti-mouse CD45 and anti-human CD45抗体。小鼠外周血单个核细胞中人CD45+细胞的比例> 20%,证实人白细胞移植成功。如图所示注射U937(人组织细胞淋巴瘤细胞)与BMP2或BMP2与k02288。目的是通过小分子抑制剂抑制BMP2信号途径阻碍Reg-Vδ2 T细胞产生和促肿瘤生长效果。结果表明:K02288联合BMP2处理则明显抑制了U937细胞的生长并显著延长生存期。
参考文献:
1. Huang C, Chen B, Wang X, et al. Gastric cancer mesenchymal stem cells via the CXCR2/HK2/PD-L1 pathway mediate immunosuppression. Gastric Cancer. 2023, 26(5):691-707.
2. Liang S, Dong T, Yue K, et al. Identification of the immunosuppressive effect of γδ T cells correlated to bone morphogenetic protein 2 in acute myeloid leukemia. Front Immunol. 2022, 13:1009709.